Vor dem Hintergrund weltweit steigenden Übergewichts verfolgen Forschende den Ursprung braunen Fettgewebes in der Embryonalentwicklung
Krems (Österreich), 12. März 2026 – Ein Team von Forscherinnen und Forschern hat einen unerwarteten Ursprung des braunen Fetts identifiziert: eine kleine Zellnische um die dorsale Aorta. Braunes Fettgewebe dient bei Säugetieren der Regulation der Körpertemperatur und rückt angesichts weltweit steigender Adipositas-Raten zunehmend in den Fokus der Forschung. Mit einer Kombination aus zeitlich kontrolliertem genetischem “Lineage-Tracing” und der RNA-Sequenzierung einzelner Zellen zeigen die Forschenden in Mausembryonen, dass Vorläuferzellen aus dieser aortennahen Region später zu braunem Fett an mehreren Körperstellen beitragen – während das bekannteste Depot zwischen den Schulterblättern (interskapuläre Region) nur in geringem Umfang aus dieser Quelle stammt. Die Arbeit wurde überwiegend an mehreren führenden Forschungseinrichtungen in Berlin durchgeführt; Teile werden nun vom Senior Scientist der Studie, Prof. Sigmar Stricker, an die Karl Landsteiner Privatuniversität (KL Krems) verlagert.
Braunes Fettgewebe – oft „braunes Fett“ genannt – ist im Körper nicht einheitlich verteilt, sondern liegt in anatomisch klar abgegrenzten Depots vor, die sich in zellulärer Zusammensetzung und Genaktivität unterscheiden. Das ist insofern relevant, als in der Forschung häufig nur ein einzelnes Depot als Modell für das gesamte braune Fettgewebe dient. Wenn Depots aber nicht dieselbe Entwicklungslinie teilen, können sie sich auch in ihrer Regulierung unterscheiden, was die Übetragung von Ergebnissen aus einer Region auf eine andere in Frage stellen würde. Die neue Studie adressiert diese Unschärfe, indem sie präzise kartiert, welche embryonalen Zellpools zu welchen Depots beitragen – und wann diese Entscheidungen währende der Entwicklung fallen.
Ein neuer Ursprung
„Frühere Studien deuteten bereits darauf hin, dass sich braune Fettdepots nicht alle auf die gleiche Weise entwickeln“, sagt Prof. Sigmar Stricker, Leiter des Fachbereichs Zellbiologie an der KL Krems. „Wir haben diese Idee nun mit zellulären Abstammungsanalysen und Einzelzell-Daten genauer überprüft und tatsächlich starke Hinweise auf einen bislang unbekannten Ursprung für Vorläuferzellen des braunen Fettgewebes nahe der dorsalen Aorta gefunden.“
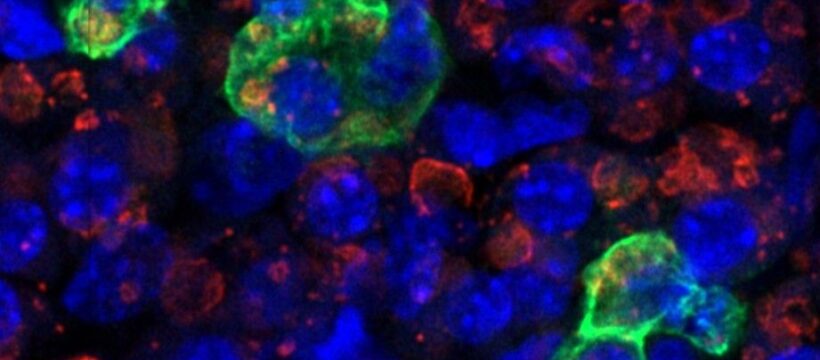
Das Team um Prof. Stricker konzentrierte sich auf Zellen, die das Gen Osr1 (einen Transkriptionsfaktor) exprimieren, und verfolgte deren Entwicklung und Migration über die Zeit. Durch Markierung Osr1-positiver Zellen in definierten embryonalen Stadien zeigte sich ein klares, depot-spezifisches Muster: Zellen aus der Osr1-Linie trugen stark zu braunem Fett unter dem Schulterblatt (subskapulär) sowie in der Halsregion (zervikal) bei, jedoch nur minimal zum großen Depot zwischen den Schulterblättern (interskapulär) – einem in Studien häufig verwendeten Referenzgewebe. Ein noch früherer Markierungszeitpunkt zeigte ebenfalls deutliche Beiträge zu den subskapulären und zervikalen Depots – ein Hinweis darauf, dass relevante Osr1-positive Vorläuferzellen bereits sehr früh in der Entwicklung vorhanden sind.
Die Einzelzell-RNA-Sequenzierung lieferte den molekularen Kontext: In einem späteren embryonalen Stadium zeigten Osr1-positive Zellen eine klarere Signatur von Vorstufen des braunen Fetts. In einem früheren Stadium hingegen wies eine Teilpopulation ein breiteres, multipotentes Profil auf – mit Genexpressionsmerkmalen typisch für Gefäß- und Muskelentwicklung. Dazu passend deutete Abstammungsanalysen der Zellen (“Lineage Tracing”) darauf hin, dass frühe Osr1-positive Zellen nicht nur zu Fettgewebe beitragen können, sondern auch zu anderen mesodermal abgeleiteten Geweben in definierten embryonalen Regionen.
Von der Aorta ins Fettgewebe
Der anatomische Hinweis auf Ursprung und Route der Vorläuferzellen ergab sich, als die Forschenden Embryonen im früheren Stadium mittels Immunfluoreszenz untersuchten: Osr1-positive Zellen waren im dorsalen Aorten-Kompartiment angereichert – einer schmalen Zone um die embryonale Aorta. Über die folgenden Tage legte das zeitaufgelöste Tracing nahe, dass sich Zellen aus der Osr1-Linie von dort in weiter rückseitiggelegene und seitliche Bereiche des Embryos ausbreiten (dorso-laterale Territorien). Dieses Muster passt zur Vorstellung von Mesoangioblasten – gefäßassoziierten, multipotenten Vorläuferzellen. Die Autorinnen und Autoren schlagen daher vor, dass dorsalaorta-assoziierte, Osr1-positive Zellen in vivo eine Quelle von Vorläufern darstellen, aus denen später mehrere braune Fettdepots entstehen können.
Ein wesentlicher Teil der experimentellen Arbeit und Infrastruktur für diese Studie war an der Freien Universität Berlin angesiedelt; weitere Expertise kam vom Max Delbrück Center Berlin, dem Max-Planck-Institut für Molekulare Genetik in Berlin sowie der Charité – Universitätsmedizin Berlin und der KL Krems. Das Deutsche Institut für Ernährungsforschung (DIfE) war ebenfalls beteiligt. Prof. Strickers heutige Basis an der Karl Landsteiner Privatuniversität verbindet diese Ergebnisse mit der breiteren Forschungsagenda der Universität und ermöglicht Folgearbeiten an der Schnittstelle von Entwicklungsbiologie und metabolischer Gesundheit.
Originalpublikation: The dorsal aortic compartment is a developmental source of brown adipose tissue in mice. S. Heider, C. Fischer, A. K. Secener, P. Vallecillo-García, G. Kotsaris, Z. G. Meisen V. Pawolski. C. Giesecke-Thiel, T. Conrad, T. J. Schulz, S. Sauer, S. Stricker. Nature Communications (2026) 17:286, doi:10.1038/s41467-025-68147-9. https://kris.kl.ac.at/en/publications/the-dorsal-aortic-compartment-is-a-developmental-source-of-brown-/
Mehr zur Forschung der KL Krems: https://www.kl.ac.at/de/forschungsblog
Karl Landsteiner Privatuniversität (Stand 03/2026)
Die Karl Landsteiner Privatuniversität (KL Krems) ist eine international anerkannte Bildungs- und Forschungseinrichtung am Campus Krems. Die KL Krems bietet eine moderne, bedarfsorientierte Aus- und Weiterbildung in der Medizin und Psychologie sowie ein PhD-Programm im Bereich Mental Health and Neuroscience an. Das flexible Bildungsangebot ist auf die Bedürfnisse der Studierenden, die Anforderungen des Arbeitsmarkts sowie auf die Herausforderungen der Wissenschaft abgestimmt. Die drei Universitätskliniken in Krems, St. Pölten und Tulln sowie das Ionentherapie- und Forschungszentrum MedAustron in Wiener Neustadt gewährleisten eine klinische Lehre und Forschung auf höchstem Qualitätsniveau. In der Forschung konzentriert sich die KL Krems auf interdisziplinäre Felder mit hoher gesundheitspolitischer Relevanz – u.a. der mentalen Gesundheit, der molekularen Onkologie und den Neurowissenschaften sowie dem Thema Wasserqualität und den damit verbundenen gesundheitlichen Aspekten. Die KL Krems wurde 2013 gegründet und von der Österreichischen Agentur für Qualitätssicherung und Akkreditierung (AQ Austria) akkreditiert. https://www.kl.ac.at/
Wissenschaftlicher Kontakt
Prof. Sigmar Stricker
Fakultät für Medizin
Karl Landsteiner Privatuniversität
Dr.-Karl-Dorrek-Straße 30
3500 Krems / Österreich
T +43 2732 7209 0761
E sigmar.stricker@kl.ac.at
Karl Landsteiner Privatuniversität
Mag. Selma Vrazalica, BA
Kommunikation, PR & Marketing
Dr.-Karl-Dorrek-Straße 30
3500 Krems / Österreich
T +43 2732 72090 237
M +43 664 883 99 603
Textredaktion & Aussendung
PR&D – Public Relations für Forschung & Bildung
Dr. Barbara Bauder-Jelitto
Kollersteig 68
3400 Klosterneuburg / Österreich
M +43 664 1576 350
L https://www.linkedin.com/company/prd-public-relations-für-forschung-bildung